病毒是科学研究中的重要工具,可用于研究基因表达和蛋白质合成等基本生物学过程。腺相关病毒(AAV)、慢病毒和噬菌体因其能够整合到宿主基因组中,被广泛用作基因治疗的载体。同样,病毒样颗粒(VLP)——一种模拟病毒结构的非感染性纳米外壳——具有高度免疫原性,被用作针对多种疾病的疫苗。它们也可以经过改造以携带治疗剂用于药物递送,并用作纳米材料和纳米器件的构建模块。
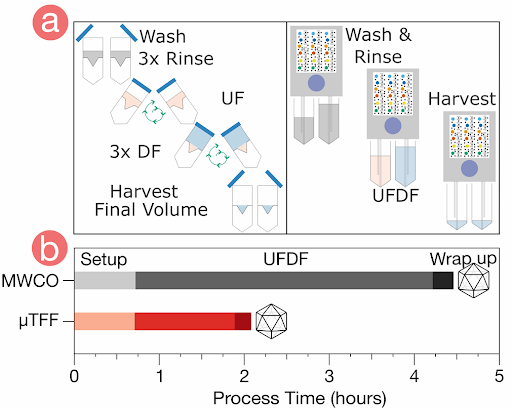
病毒生产工作流程包括多个阶段:扩增、收获、纯化和制剂。该过程从培养被病毒感染的宿主细胞(哺乳动物细胞、昆虫细胞或细菌细胞)开始。一旦完成扩增,便从培养基或宿主细胞碎片中收获病毒颗粒。随后进行纯化以去除污染的蛋白质、核酸或培养基成分。最后,将纯化的病毒进行制剂以备储存或下游应用,这需要进行样品浓缩和透析过滤(或缓冲液更换)。在收获阶段,为了对扩增的病毒进行部分纯化,同样需要这些步骤。
VLP生产与制剂工作流程
选择病毒收获和制剂方法时,必须考虑几个因素。过程的温和性对于确保最终产品的质量、稳定性和收率至关重要。此外,该方法必须能够从实验室研究放大到工业化生产规模,这需要在高生产率和成本效益之间取得平衡。时间效率也很关键,因为处理延迟会导致收率降低和成本增加。下表概述了病毒收获和制剂的常用方法。
| 考量因素 | 离心法 | 色谱法 | 沉淀法 | 超滤法 |
|---|---|---|---|---|
| 温和性 | ||||
| 可放大性 | ||||
| 收率 | ||||
| 时间效率 | ||||
| 成本效益 |
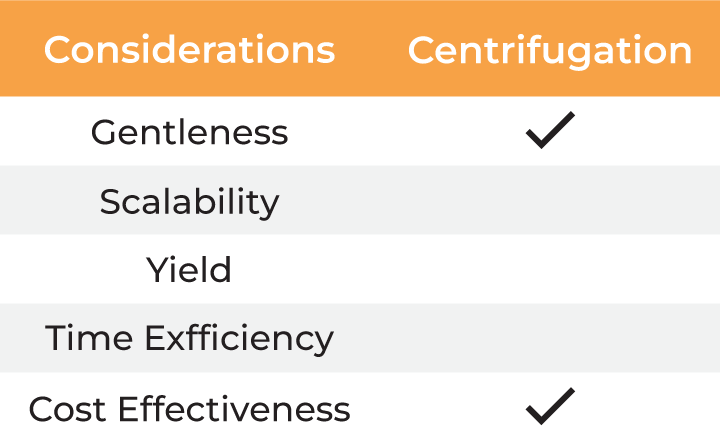
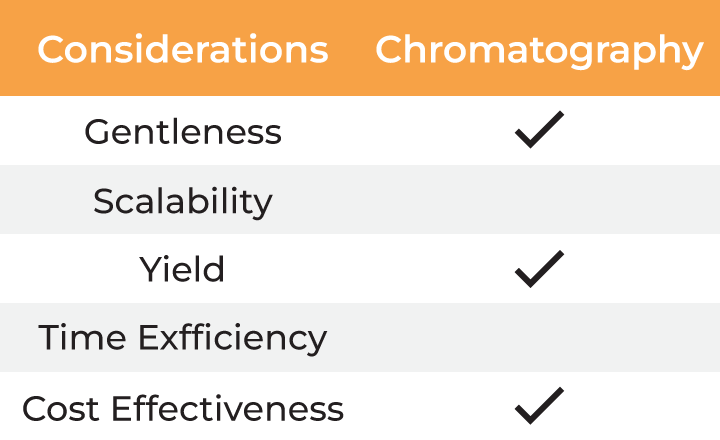
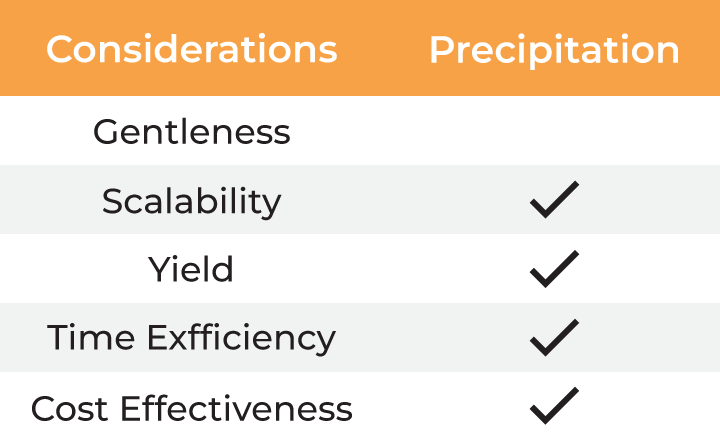
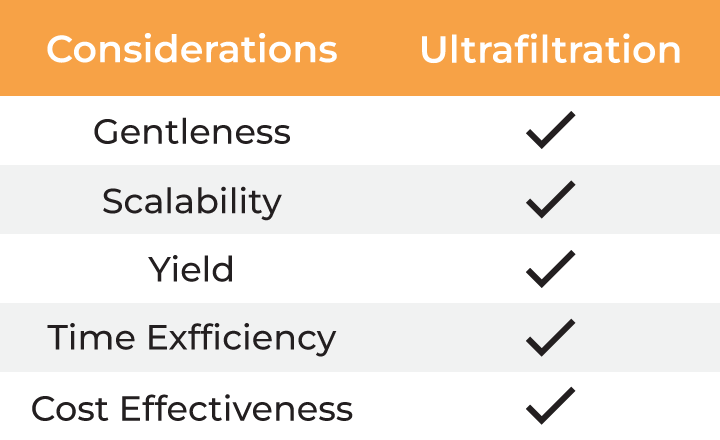
表:病毒收获与制剂方法对比
与传统方法相比,超滤法能够满足病毒收获和最终制剂的所有考量因素。然而,实验室规模常用的超滤形式——死端过滤(DEF),由于样品不循环而导致膜上形成浓度梯度,从而受到限制。这会减慢过滤过程,并可能因聚集而导致物料损失。此外,监控浓缩进程或混合样品的唯一方法是定期中断离心,这使得它成为一种需要手动操作的方法,并进一步增加了处理时间。最后,死端离心装置缺乏可扩展性,只能处理有限的体积。
与DEF相关的限制被切向流过滤(TFF) 有效克服。TFF通过持续的样品再循环避免滤饼形成,确保高过滤速率。TFF还具有可扩展性的优势,并能同时进行缓冲液更换和样品浓缩。然而,传统的TFF系统占地面积大,滞留体积达数十至数百毫升,不适合实验室规模的应用。为了克服这一挑战,Formulatrix 开发了 µPulse®——一款专为实验室规模体积设计的微型化TFF系统。
使用 aµtoPulse - TFF 系统进行高通量病毒处理
aµtoPulse® 是一款全自动、高通量的 TFF 系统,拥有全球最低的滞留体积,仅为 250 µL。每次运行可处理多达 54 个样品,最多可并行处理 4 个样品。设计灵活,可处理 0.5 mL 至 100 mL 的起始体积,并能将样品浓缩至 250 µL,精度为 ±25 µL。该系统支持多达四个外部缓冲液输入或板载锥形管,可实现自动化的多缓冲液透析过滤。
采用双泵的先进芯片设计,其在处理敏感病毒和病毒样颗粒(VLP)时,渗透物流速比 µPulse 快达 1.7 倍,同时最大限度地减少了剪切力。芯片提供 mPES(5-300 kDa)和 RC(5-100 kDa)膜,确保与广泛的样品兼容。
每个工作站提供独立的跨膜压力(0-32 psi)调节和监测,使用户能够完全控制过程的温和性与效率。直观的基于浏览器的软件支持远程方案设置、监控和控制,并提供符合 21 CFR Part 11 法规(适用于 GMP 环境)的安全数据管理。
网络研讨会

资源
体验微型化 µPulse - TFF 系统在蛋白质样品浓缩和缓冲液更换中的高效、快速和温和特性。
来自 Dyno Therapeutics