样品浓缩与缓冲液交换是任何制备规模蛋白质生产(无论是用于结构生物学还是普通生物化学需求)不可或缺的环节。这些步骤是确保纯化步骤之间满足特定层析要求所必需的。即使在纯化之后,也必须将蛋白质在特定缓冲液中配制到适当浓度,以确保其结构完整性以及下游应用的有效性。类似地,通过控制性去除变性剂以实现溶解包涵体的体外复性时,也可能需要进行缓冲液置换。
鉴于这些步骤的重要性,在选择蛋白质处理方法时,必须考虑诸如过程温和性、时间效率、可放大性和成本效益等因素。表1和表2分别概述了用于蛋白质浓缩和缓冲液置换的典型方法:
| 考量因素 | 柱层析 | 冷冻干燥 | 蒸发 | 吸附 |
超滤 死端过滤 TFF |
|---|---|---|---|---|---|
| 温和性 | ✔ | ✔ | ✔ ✔ | ||
| 可放大性 | ✔ | ✔ | ✔ | ✔ | ✔ |
| 时间效率 | ✔ | ||||
| 成本效益 | ✔ | ✔ | ✔ ✔ | ||
| 自动化 | ✔ |

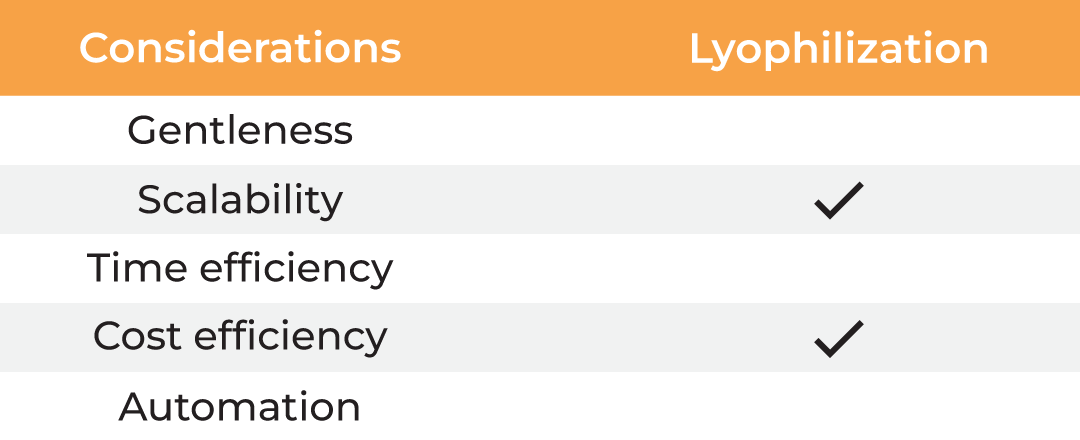



表1. 蛋白质浓缩方法
与传统方法相比,超滤技术能够满足蛋白质浓缩和缓冲液交换的所有考量。然而,死端超滤由于样品不进行再循环,会在膜表面形成浓度梯度。这会减慢过滤过程,并可能因聚集而导致物料损失。监控浓缩进程或混匀样品的唯一方法是定期中断离心,这使得它成为一种手动方法,并进一步增加了处理时间。最后,死端离心装置缺乏可放大性,只能处理有限的体积。
切向流过滤有效地解决了这些问题,它是超滤的另一种形式,涉及样品的持续再循环,从而避免了滤饼层的形成并确保了高过滤速率。切向流过滤还提供了可放大性以及同时进行缓冲液交换和样品浓缩的优势。然而,传统的切向流过滤系统占地面积大,死体积达数十至数百毫升,使其不适合实验室规模的应用。
| 考量因素 | 柱层析 | 稀释 | 平衡透析 |
超滤 死端过滤 TFF |
|---|---|---|---|---|
| 温和性 | ✔ | ✔ | ✔ | ✔ ✔ |
| 可放大性 | ✔ | ✔ | ✔ | |
| 时间效率 | ✔ | |||
| 成本效益 | ✔ ✔ | |||
| 自动化 | ✔ |

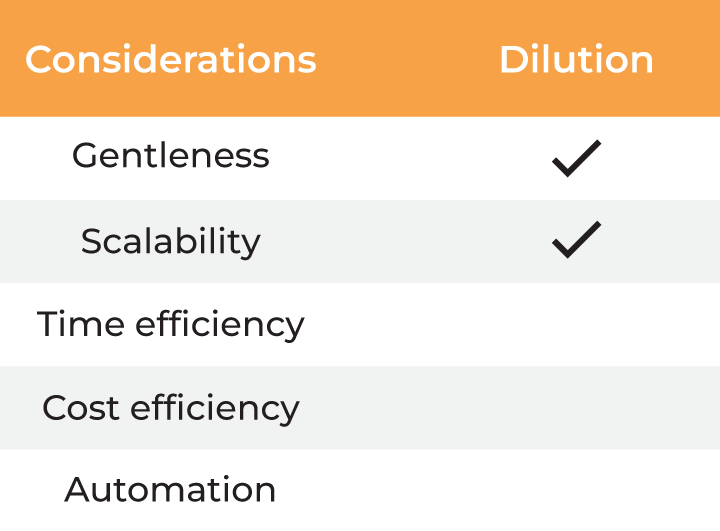

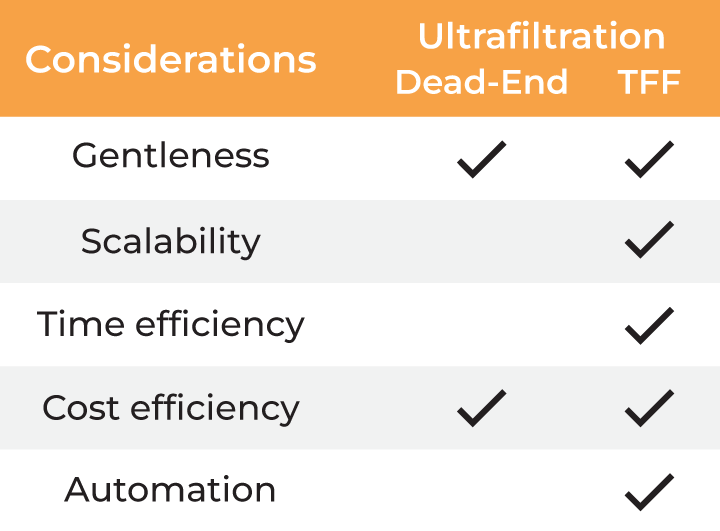
表2. 缓冲液交换方法
使用 µPulse - TFF 系统进行蛋白质处理
使用 aµtoPulse - TFF 系统进行高通量蛋白质处理
aµtoPulse® 是一款全自动、高通量的切向流过滤系统,具有全球最低的250微升死体积。它每轮可处理多达54个样品,最多可并行处理4个样品。设计灵活,可处理起始体积在0.5毫升到100毫升之间的样品,并能将样品浓缩至250微升,精度达±25微升。系统支持最多四个外部缓冲液输入或台上锥形管,可实现自动化多缓冲液渗滤。
其先进的芯片设计配备双泵,滤出液流速比µPulse快达1.7倍,同时最大限度减少了剪切力,这对于精细蛋白质和复合物尤为重要。芯片提供mPES膜(5-300 kDa)和RC膜(5-100 kDa),确保与多种样品的兼容性。
每个工位都提供独立的跨膜压(0-32 psi)调节和监控,让用户完全控制工艺的温和性与效率。直观的、基于浏览器的软件支持远程方案设置、监控和控制,其安全的数据管理功能符合GMP环境下21 CFR Part 11的要求。
Webinars
Learn a fast, gentle, and automated approach for harvesting extracellular VLPs as well as refolding, and formulating various proteins using the µPulse.
Experience the single-step and scalable purification of ADCs and other macromolecules modified with small molecules using the µPulse.
Application Notes
Uncover the ease of use, scalability, and reusability of µPulse for lab scale formulation of recombinant L-asparaginase and other biomolecules.
Learn about the time efficiency, cost effectiveness and gentleness of µPulse for refolding denatured proteins compared to equilibrium dialysis.